Wenn es um Erdgas geht, dürfen Sie damit nicht nicht vertraut sein, und heutzutage kann kein Haushalt ohne sie kochen. Die Hauptkomponente von Erdgas ist Methan, eine der einfachsten Kohlenwasserstoffverbindungen. Die Beschleunigung der Entwicklung und Nutzung von Methan ist der Schlüssel, um die grüne und nachhaltige Entwicklung der Energie- und chemischen Industrie zu realisieren. Zusätzlich zu seiner direkten Verwendung als Brennstoff kann Methan auch als C1-Ressource verwendet werden, dh ein Molekül, das ein Kohlenstoffatom enthält und weiterhin umgewandelt werden kann, um hochwertige Chemikalien wie Methanol, Formik, herzustellen Säure und so weiter. Methan kann in Sauerstoff verbrannt werden, um Wasser und Kohlendioxid zu bilden. Ist es ohne Verbrennung möglich, die Kohlenwasserstoffbindungen von Methanmolekülen unter milden Bedingungen zu aktivieren und zu konvertieren? Die Antwort ist ja! Dies ist die "Heilige Gral" -Reaktion im Bereich der Katalyse. Reaktionen, die mit dem "Heiligen Gral" verbunden sind Ausbeuten und niedrige Selektivität. Diese Herausforderungen erschweren es, diese Reaktionen zu realisieren, aber wenn sie erfolgreich erreicht werden können, werden sie zu erheblichen Durchbrüchen in der wissenschaftlichen Forschung und in der industriellen Anwendungen führen.

1. Verschiebungen bei der Umwandlung von Methan bei niedrigen Temperaturen Es ist sehr schwierig, Methan direkt in andere nützliche Chemikalien mit kostengünstigem Sauerstoff bei niedrigen Temperaturen oder sogar Raumtemperatur umzuwandeln. Warum ist das so? Schauen wir uns die Natur von Methan und Sauerstoff an. Die chemische Struktur von Methan enthält vier identische Kohlenstoffhydrogenbindungen (CH), die eine stark symmetrische orthotetraedrische Konfiguration bilden, und jede CH3-H-Bindung von Methan hat eine Bindungsenergie von bis zu 435 kJ/mol. Wir können uns die CH -Bindung von Methan als eine besonders starke Quelle vorstellen. Diese Frühling ist sehr straff und erfordert viel Kraft, um sich zu dehnen. In der Chemie ist diese "Kraft" die Energie, die erforderlich ist, um die CH -Bindung zu brechen. Diese hohe Bindungsenergie macht Methans CH -Bindungen thermodynamisch stabil und sehr schwierig zu brechen oder unter normalen Bedingungen zu reagieren. Andererseits werden bei chemischen Reaktionen reaktive Gruppen normalerweise unter polarer Wechselwirkung erzeugt (polare Wechselwirkung ist das Phänomen, dass ein Molekül ein Ende positiv geladen und das andere negativ geladen ist), während die symmetrische Struktur und die nichtpolare Natur des Methanmoleküls vorhanden ist Es wird durch eine solche Polarität erzeugt (gemäß der molekularen Konfiguration hat ein Molekül mit einer Symmetrieebene keine Polarität) und kann keine reaktiven Gruppen liefern. Daher ist die Aktivierung und Umwandlung von Methan sehr schwierig und erfordert normalerweise harte Erkrankungen wie hohe Temperaturen (600-1100 ° C) oder einige "Extremophile" wie Super-Stadel-Säuren und freie Radikale, um die Aktivierung von Methan zu unterstützen. Daher liegt die Hauptschwierigkeit bei der Realisierung der niedrigen Temperaturaktivierung von Methan und Sauerstoff darin, wie die CH-Bindung von Methan, dh die "Frühling" in der CH-Bindung, aktiviert werden kann. 2.Das Wunder des Katalysators Wissenschaftler haben eine gute Lösung für dieses Problem entwickelt und sich für einen Katalysator entschieden, um Methan bei niedrigen Temperaturen zu aktivieren (ein Katalysator ist eine Chemikalie, die sich nicht vor oder nach einer Reaktion ändert, aber die Reaktion beschleunigt von Energie, die injiziert werden muss, damit die Reaktion stattfinden kann). Im Jahr 2023 berichtete die Journal Nature -Katalyse über den Prozess der direkten Umwandlung von Methan mit Sauerstoff in C1 -Oxide (Methanol (CH3OH), Ameisensäure (HCOOH) und Methylenglykol (Hoch2OH)) unter Verwendung eines spezifischen Molybdennennids (MOS2) (MOS2) (MOS2) (MOS2) (MOS2) (MOS2) (MOS2) (MOS2) (MOS2) (MOS2)) Katalysator bei 25 ° C. Eine Methanumwandlung von 4,2% und fast 100% C1 -Sauerstoffaten wurde durch Verwandeln von Methan und Sauerstoff in wertvolle C1 -Sauerstoff unter Umgebungsbedingungen erreicht. Dieser MOS2 ist der einzige Katalysator, der bisher gemeldet wurde und die die Umwandlung von Methan und Sauerstoff der Raumtemperatur realisieren kann. Dies alles liegt an der einzigartigen Geometrie und elektronischen Struktur des MO -Standorts am Rand des MOS2. Diese MO -Stelle hat eine hohe Aktivierungsaktivität in Richtung Sauerstoff in einer wässrigen Umgebung und bildet die magische O = Mo = O* -Spezies. Diese Spezies erleichtert die Bindung der Kohlenstoffhydrogen leichter zu brechen und reduziert die Aktivierungsenergie der CH-Bindung von Methan, wodurch die Reaktivität von Methan erheblich erhöht wird und damit die Aktivierung von Methan und Sauerstoff mit niedriger Temperatur realisiert wird. Diese Entdeckung wird mehr Möglichkeiten für die zukünftige Energieversuche und den Umweltschutz bieten und uns ein tieferes Verständnis für die erstaunliche Rolle von Katalysatoren und Hilfsmitteln vermitteln.
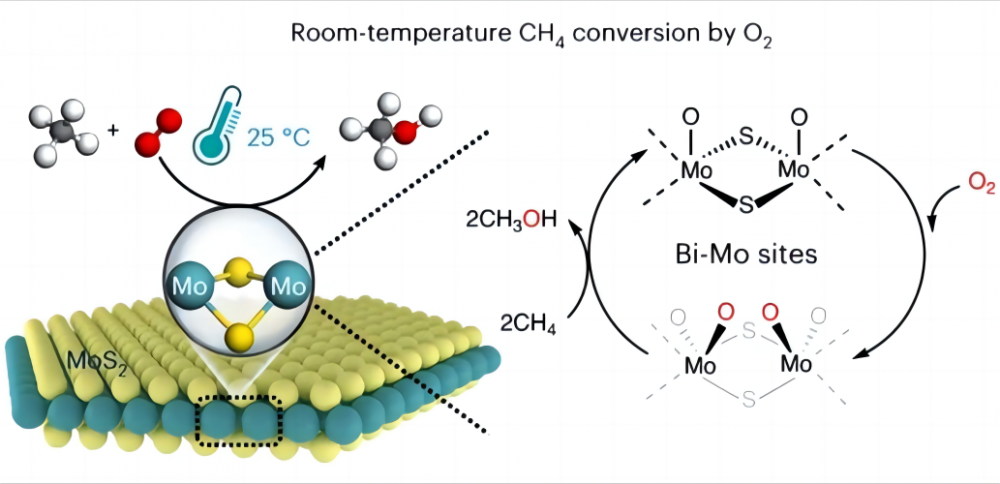
3. signifikante strategische Bedeutung der Aktivierung von Methan mit niedriger Temperatur Die direkte katalytische Umwandlung von Methan und Sauerstoff bei Raumtemperatur und die Umwandlung von Methan in Erdgas in andere nützliche Chemikalien kann die Nutzungsrate von Erdgas erheblich verbessern, den Abfall reduzieren und die Umwelt besser schützen und die nachhaltige Entwicklung von Energie besser realisieren . Zweitens ist Methan als Gewächshausgas in seinem Beitrag zur globalen Erwärmung an zweiter Stelle auf Kohlendioxid. Wenn Methan in andere Substanzen umgewandelt werden kann, kann es uns helfen, die Emission von Luftschadstoffen (z.




